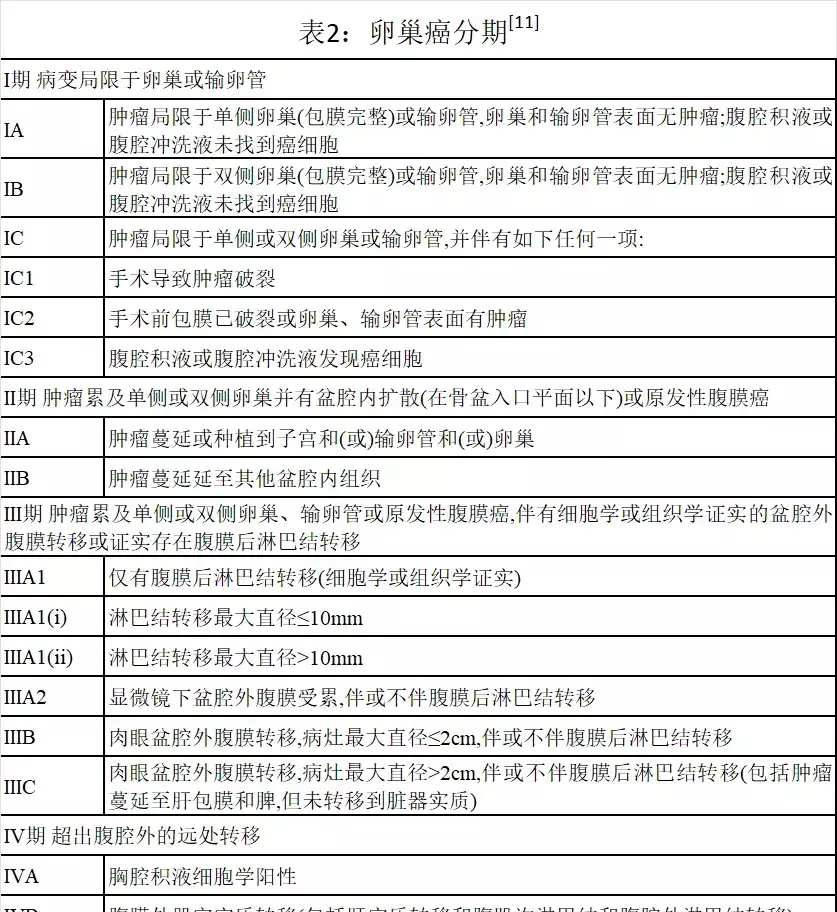
卵巢癌发病率位于女性生殖系统恶性肿瘤第3位,致死率居妇科恶性肿瘤之首[1],全世界每年有31.4万例病例和20.7万例死亡[2]。约70%的患者在初诊时已进展至晚期,5年生存率不足40%。目前卵巢癌从疾病筛查到综合治疗,从多学科协作到疾病全程管理都面临着一定的挑战,如何能使卵巢癌患者延长生命周期、提高生活质量从而最大获益是医疗工作者所共同追求的目标。因此《医师报》特别邀请宁波大学附属第一医院管玉涛教授、浙江大学医学院附属二院周建维教授、浙江省人民医院寿华锋教授、浙江大学附属妇产科医院张松法教授和、江省肿瘤医院张英丽教授共同深入交流卵巢癌筛查和综合治疗相关临床经验及建议。
1
管玉涛教授:卵巢癌早期筛查面临挑战,新型标志物有望提高筛查效率
卵巢癌早期诊断可为患者带来生存优势,即使是侵袭性高级别、低分化或未分化肿瘤,在I/II期诊断时,其5年生存率高达74%,与III/IV期患者27%的5年生存率相比大大提高[3],因此卵巢癌的早期筛查诊断尤为重要。但是目前卵巢癌的早期筛查面临诸多难点。首先,卵巢的体积较小且位于盆腔深处,其解剖学特点使其早期病变不易被察觉,加之许多侵袭性卵巢癌起源于输卵管上皮细胞,本身即具有不容易成像的特点,这些特点均导致了卵巢癌影像学检查遗漏和误诊的概率较大。其次,卵巢肿瘤缺乏特异性标志物,炎症或者其他器官肿瘤均可以导致相应肿瘤标志物的升高;同时,卵巢癌是所有人体肿瘤中类型最多、组织成份最复杂的肿瘤,这一特点也使得并非所有卵巢癌亚型均可通过肿瘤标志物进行筛查。
卵巢癌目前缺乏早期有效的筛查,但并非意味不进行筛查。尤其对于卵巢癌高危人群,特别是有卵巢癌家族史或BRCA1和BRCA2阳性人群,建议每6个月进行一次超声检查和血清CA125 检查[4],也可在此基础上联合其他肿瘤标志物如HE4进行筛查,以增加卵巢上皮性肿瘤的检出率。目前,全球正在研究几种新的生物标志物和筛选策略,并可能在未来带来希望。包括DNA甲基化生物标志物、游离DNA、循环肿瘤DNA(ctDNA)、糖基化Ca125、Olink生物标志物、以及多癌种早期检测(MCED)生物标志物策略[2]。新的标志物的探索研究有望在寻求有效的卵巢癌筛查策略方面取得巨大进展。
2
周建维教授:卵巢癌筛查方法局限性与获益性并存,影像学、血清、基因三管齐下
卵巢癌早期的筛查十分困难,到目前为止并没有较为有效的早筛方法,因此约70%的卵巢癌发现时已到达晚期。但假如能早期筛查出卵巢癌将对患者的治疗提供较大的帮助,使患者显著获益并长期生存,因此卵巢癌的筛查仍具有一定的必要性。目前对卵巢癌的筛查最常见的方法就是B超[5],B超可以提供有关卵巢形态、血管和内部特征信息,在区分良恶性卵巢肿瘤时有较高的敏感性和特异性,若卵巢包块实性成分居多且血流丰富,则提示包块恶性的可能性较大。其次是CT和核磁共振[6],CT对于判断卵巢肿块的是否实性或者囊实性也有帮助;增强核磁共振或者与CT检查相结合,都能够有助于肿块性质的确定以及判断其血流的状况,从而有助于判断其良恶性。血液肿瘤标志物在卵巢癌诊断方面也具有一定价值,不同病理类型的卵巢癌可具有不同的肿瘤标志物,CA125及HE4是上皮性卵巢癌中应用价值最高的肿瘤标志物,AFP 、β-HCG、NSE、LDH和CA199可用于卵巢恶性生殖细胞肿瘤的辅助诊断,胃肠道转移性肿瘤可出现CA199及CEA升高,罕见非妊娠性卵巢绒癌也会出现HCG升高,另外ROMA指数是将CA125和HE4血清值与患者绝经状态相结合的一个评估模型,可帮助评估卵巢恶性肿瘤的风险。这些肿瘤标志物都具有一定的诊断卵巢恶性肿瘤的临床参考意义。但假如能将影像学和血清肿瘤标志物两者相结合则能显著提高卵巢恶性肿瘤诊断的准确率,更加精准地对卵巢癌进行早期筛查。
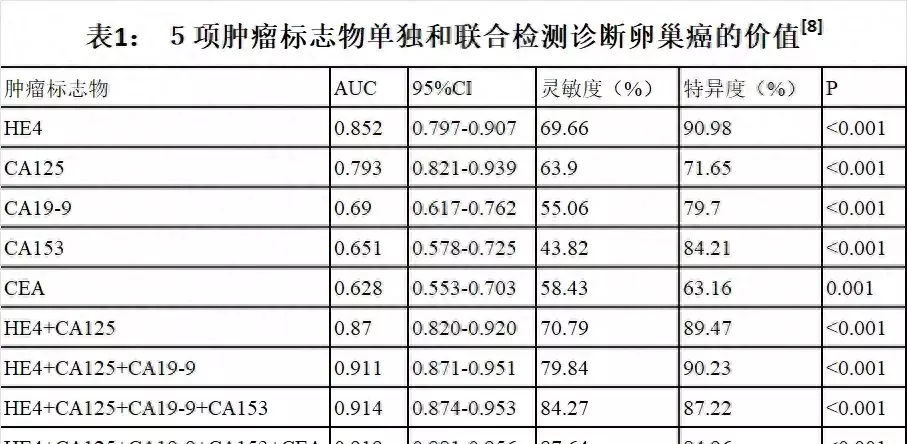
约20%-25%的上皮性卵巢癌与遗传因素相关,对于有BRCA基因突变、Lynch综合征或者两个一级亲属以上患有卵巢癌的高危人群,首先要增加其筛查频率,其次可以在适当年龄段进行预防性输卵管卵巢切除术,从而降低卵巢癌的发生率。
3
寿华锋教授:综合治疗,全程管理,使卵巢癌患者最大获益
规范的综合性治疗和全程管理对于卵巢癌患者的治疗以及预后至关重要。即使70%的卵巢癌患者发现时已经是晚期并且预后较差,但是随着治疗手段不断的跟进,大部分患者的治疗效果仍较好。此时,患者面临最大的风险时疾病复发或者再次进展,因此综合治疗和全程管理尤其重要。综合治疗减少了不同部门之间分工的分割,如手术、化疗、放疗、生物治疗、免疫治疗包括支持治疗可以一并进行,而非割裂开来。从而能够根据病人病情特点或者病人的特殊需求进行个体化管理以及更加规范化治疗,最终达到提高患者生存质量、延长患者生命周期两个目的。
此外从人文的角度出发,综合性治疗有助于提高患者的医从性,当患者病情进展或者复发时,能够及时规范就医,避免乱就医、乱服药的发生,避免病情延误,减少不必要的损失,使患者能够长期获益。
4
张松法教授:多学科诊治经验丰富,机制评价有待完善
鉴于卵巢癌的特点,即:诊断时大部分患者已经进入晚期、广泛转移以及复发率较高,多学科协商诊疗的模式非常适合这一疾病的管理。从诊断到手术时机选择到术后并发症处理,以及复发后治疗决策问题可以通过多学科诊疗进行流程化管理。对于如何系统且高效的完成多学科诊疗,主要有以下两点:首先是主诊医生全程负责和把控,避免由于医院科室分工精细导致医生对患者的病情把控缺失;其次是确保合作科室和支持技术齐全,能够满足各种治疗手段如手术、化疗、放疗、生物治疗、免疫治疗均可进行。对于有特殊需求,如有生育需求的患者也能够联合其他科室如生殖科等一并进行相关治疗和辅助措施。
对于多学科诊疗(MDT)的实行仍存在一些难点。首先,在主诊医生全程负责的体系背景下,医生与患者建立一个良性的或者互相信任的关系是非常重要的,而这往往充满一定挑战。其次,多学科团队机制的建立以及人员配置应保持相对稳固,成员之间彼此能够充分了解并且治疗理念也应较为一致。其三,目前对于MDT机制的考评仍面临着挑战,如何推进规范化的MDT讨论或者协作,以及如何评价病人诊治效果、团队运转效果和卫生经济学效果都是目前亟待解决的问题。
5
张英丽教授:制定个性化的治疗,留存患者生育功能
卵巢癌患者能否留存生育功能是需要多方面评估和讨论的问题。目前认为对有生育要求的年轻早期卵巢癌患者实施保育治疗安全有效,可获得良好的妊娠结局[9]。但需严格掌控留存生育治疗的手术指征。首先,从患者角度出发,应确保患者进行了保生育的手术以后,能够保证肿瘤的治疗效果;其次,应确认患者的年龄、病理类型及手术病理分期。2014 年中华医学会妇科肿瘤分会制定的《妇科恶性肿瘤留存生育功能临床诊治指南》指出保育治疗的筛选标准:①患者年龄<40 岁,渴望生育;②患者对FSS带来的肿瘤复发风险充分知情;③病理分化程度为高分化;④病理提示病变局限在一侧卵巢,对侧卵巢和子宫无异常;⑤腹腔细胞学检查阴性;⑥“高危区域”(子宫直肠陷凹、结肠侧沟、肠系膜、大网膜和腹膜后淋巴结)探查及多点活检均阴性;⑦有随诊条件;⑧完成生育后视情况再行子宫及对侧附件切除术[10]。在满足留存生育手术的前提下,选择安全可行的手术方式并注意术中操作,术后合理辅助化疗、科学应用卵巢功能保护药物及辅助生殖技术,从而使患者长期获益。